JANO
Un estudio internacional del CIBERER, el IDiPAZ y el UAM-CSIC pone de manifiesto que mutaciones en el exón específico de músculo del gen FXR1 causan esta enfermedad.
Un grupo de investigadores del CIBERER, el IDiPAZ y el Instituto de Investigaciones Biomédicas Alberto Sols (UAM-CSIC) ha liderado un estudio internacional que ha puesto de manifiesto que mutaciones en el exón específico de músculo del gen FXR1, cuya relación con una patología humana no había sido demostrada anteriormente, son causantes de una miopatía congénita en humanos y en ratones. La investigación ha sido publicada en Nature Communications.
Fragile X relacionado 1 (FXR1), Fragile X relacionado 2 (FXR2), y Fragile X retraso mental 1 (FMR1), conforman una familia de genes homólogos involucrados en la regulación postranscripcional del ARNm. Los productos proteicos de estos genes (FXR1P, FXR2P y FMR1P, respectivamente) contienen dominios de unión de ARN KH y RGG y se ha demostrado que están asociados con ribonucleopartículas mensajeras polisomales.
El FXR1 se expresa en una amplia variedad de tejidos y está sujeto a empalmes alternativos. Por consiguiente, se han identificado siete isoformas diferentes de ARNm FXR1, algunas de las cuales son específicas del tejido. Mientras que la mayoría de los tejidos expresan variantes del FXR1P que van de 70 a 80 kDa, el músculo cardíaco y esquelético sólo genera isoformas del FXR1P de 82 y 84 kDa , que contienen un exón adicional de 81-nucleótidos (exón-15) exclusivo para estas variantes. La incorporación del exón-15 en las variantes P82,84 lleva a la inserción en el marco de 27 aminoácidos adicionales que abarcan un motivo rico en arginina que también está presente en FXR2P, y es similar a la señal de localización nucleolar de la proteína HIV1-REV10.
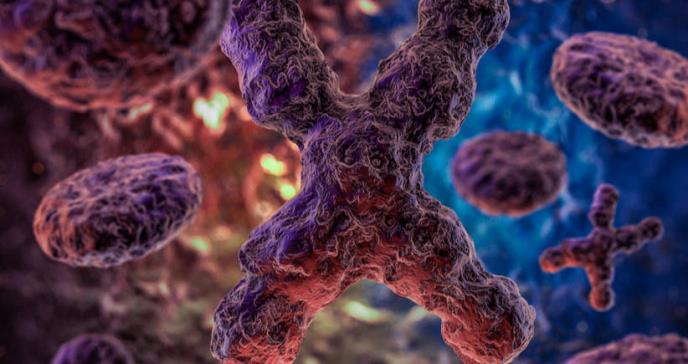
Foto original del estudio publicado en Nature.com[/caption]
Tanto el empalme distintivo del exón-15 en los tejidos musculares como su correspondiente secuencia de aminoácidos se conservan a lo largo de la evolución de los vertebrados. Sin embargo, la expresión de las proteínas FXR1P no es uniforme entre todas las células del linaje miogénico. Durante la diferenciación muscular, los mioblastos sintetizan todas las isoformas del FXR1P, mientras que los miotubos sólo expresan variantes del P82,84, aunque en mayor proporción que sus células precursoras.
Como se puede leer en el artículo original, los investigadores notaron que la inactivación constituiva de Fxr1 en modelos animales, causaba mortalidad neonatal debido a insuficiencia cardíaca y/o respiratoria secundaria a la pérdida de la estructura de las miofibras. Además, el derribo de FXr1 se puedo identificar como defectos musculares específicos y en un desarrollo anormal del musculo cardíaco, también en modelos animales. Las células musculares de pacientes con distrofia muscular facioescapulohumeral también se describieron con niveles reducidos de P82,847. Sin embargo, no se ha demostrado previamente que ninguna enfermedad humana esté asociada con mutaciones FXR1. Por ello en el estudio se reporta que rlas mutaciones recesivas en el exón-15 del FXR1 causan defectos musculoesqueléticos de severidad variable en humanos y ratones.
Los pacientes con esta enfermedad rara pueden presentar un cuadro clínico variable, que oscila desde una disminución del tono muscular grave que es letal en los primeros meses tras el nacimiento a otro más moderado, con alteraciones musculares crónicas compatibles con la vida. La nueva miopatía congénita descrita es de tipo "multi-minicore", lo que quiere decir que en las fibras musculares aparecen múltiples zonas en las que se pierde su estructura y por tanto no son plenamente funcionales. El trabajo también demuestra que la proteína FXR1 mutante que se fabrica en la forma más grave de esta enfermedad se acumula en el interior de las fibras musculares formando gránulos citoplasmáticos.
El trabajo ha sido liderado por Víctor Luis Ruiz-Pérez, del Instituto de Investigaciones Biomédicas Alberto Sols (UAM-CSIC), y Pablo Lapunzina, del INGEMM del Hospital La Paz, ambos del IDiPAZ y del CIBERER. En el estudio ha sido esencial la participación de investigadores de Canadá, Estados Unidos y Egipto y otros grupos del Hospital Universitario La Paz, la UAM, el IIS-Fundación Jiménez Díaz, el Hospital Ramón y Cajal de Madrid, el Hospital Vall d’Hebron de Barcelona, la Universidad Pablo de Olavide de Sevilla y el CIBERER.