Se identificó una disminución en la expresión de tres genes: TMSB4X, asociado a la reparación tisular y cuyo déficit podría explicar el daño renal característico de la nefritis lúpica.
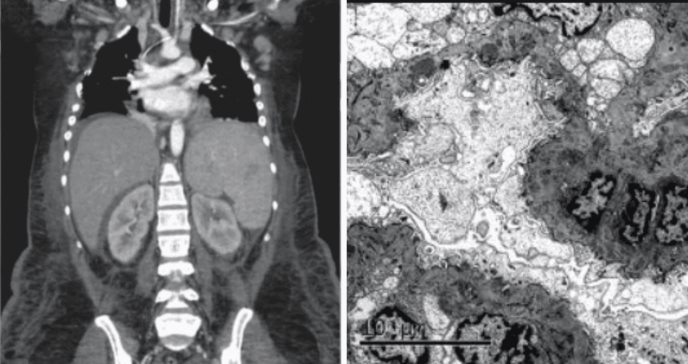
El Lupus Eritematoso Sistémico (LES) es una enfermedad autoinmune crónica. Esta condición se caracteriza por una respuesta inmune desregulada que ataca los tejidos sanos, provocando inflamación y daño en órganos como los riñones, la piel, el corazón y las articulaciones.
A pesar de los avances en la investigación, la etiología del LES sigue siendo desconocida, lo que dificulta el desarrollo de tratamientos efectivos.
En este estudio (Coral D. et al), se exploró cómo los sistemas inmunes innato y adaptativo contribuyen a la patología del LES, con el objetivo de identificar biomarcadores que puedan servir para mejorar el diagnóstico y el tratamiento.
Para ello, se emplearon herramientas bioinformáticas que permitieron comparar la expresión génica en pacientes con LES frente a individuos con una respuesta inmune normal.
El análisis se justificó en el conjunto de datos GSE 51997, obtenido del repositorio Gene Expression Omnibus. Se aplicaron técnicas de BioOptimática, incluyendo Optimización Multi-Criterio Individual (MCO), Árbol de Expansión Mínima (MST) y Ontología Génica (GO), para identificar genes diferencialmente expresados (DEGs) relevantes.
Además, se realizó una revisión bibliográfica exhaustiva para validar los hallazgos y explorar su relevancia biológica.
El estudio identificó cinco genes con patrones de expresión alterados en pacientes con LES: TMSB4X, EEF1A1, B2M, ISG15 e IFFI44L. Tres de ellos (TMSB4X, EEF1A1 y B2M) mostraron una disminución en su expresión en comparación con los controles, mientras que ISG15 e IFFI44L presentaron un aumento.
Entre estos genes, TMSB4X y EEF1A1 emergieron como candidatos prometedores para nuevos biomarcadores del LES. La subexpresión de TMSB4X se asoció con un deterioro en la función renal, lo que sugiere su posible papel en el desarrollo de nefritis lúpica.
Por otro lado, la subexpresión de EEF1A1 podría estar relacionada con alteraciones en la transcripción del Interferón II, una citocina clave en la regulación de la tolerancia inmune.
Los resultados obtenidos dejan ver que es necesario integrar enfoques computacionales y experimentales en la investigación de enfermedades tan complejas como el LES. La identificación de TMSB4X y EEF1A1 como posibles biomarcadores abre nuevas opciones para explorar mecanismos moleculares específicos de la enfermedad y diseñar terapias más dirigidas.