Los perfiles de las células madre de los síndromes mielodisplásicos podrían considerarse como un biomarcador para las guías secundarias de terapia.
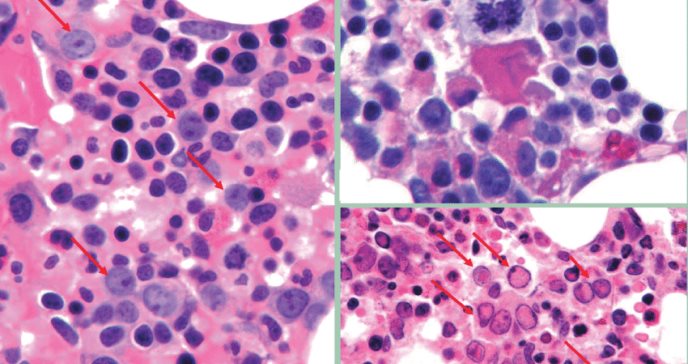
Investigadores del Centro Oncológico MD Anderson de la Universidad de Texas (Estados Unidos) han descubierto que la resistencia al tratamiento en pacientes con síndromes mielodisplásicos (SMD) está causada por dos clases distintas de células madre e identificaron posibles enfoques terapéuticos dirigidos a estas células.
Sus hallazgos, que podrían tener importantes beneficios para los pacientes con progresión de la enfermedad, según publican en la revista 'Nature Medicine'.
Esta investigación, que abarca estudios preclínicos y clínicos, representa el mayor análisis realizado hasta la fecha de muestras de pacientes con SMD.
Si se validan en ensayos clínicos más amplios, los datos sugieren que los perfiles de las células madre de los SMD podrían considerarse como un biomarcador para guiar el diseño o la elección de líneas secundarias de terapia.
Estos resultados indican que el tratamiento con venetoclax induce la muerte de las células madre en uno de los grupos de SMD.
"La mayoría de los casos de SMD no responden a las terapias actuales o recaen" recuerda la doctora Simona Colla, profesora asociada de Leucemia y autora principal del estudio.
"Este estudio aporta nuevos conocimientos sobre las causas del fracaso terapéutico y de la progresión de la enfermedad en los SMD y posiblemente proporcione opciones de tratamiento específicas para estos pacientes".
Los síndromes mielodisplásicos son un grupo de enfermedades en las que la médula ósea no produce suficientes células sanguíneas sanas.
Las enfermedades se originan en unas células conocidas como células madre hematopoyéticas (HSC) que pueden perseverar e incluso crecer durante el tratamiento estándar con agentes hipometilantes (HMA).
Aproximadamente la mitad de los pacientes con SMD tratados con HMA desarrollarán resistencia a estos fármacos y progresarán a una leucemia mieloide aguda secundaria (LMAs).
Los pacientes en los que la terapia ha fracasado suelen sobrevivir solo de cuatro a seis meses y tienen tasas de respuesta completa más bajas que la terapia estándar, dijo el doctor Guillermo García-Manero, profesor de Leucemia.
Los investigadores analizaron más de 400 muestras de pacientes con SMD tomadas en diferentes fases de la enfermedad. Mediante el uso de perfiles moleculares integradores de las HSC, descubrieron que las HMA eliminaban las células cancerosas maduras, pero dejaban vivas las células madre, lo que provocaba la recaída de la enfermedad.
La comparación de las muestras de médula ósea de pacientes no tratados con las de donantes sanos reveló que las muestras de SMD podían dividirse en dos grupos en función del perfi l de esas células madre.
Las muestras de uno de los grupos de SMD presentaban un patrón anormal de mayor frecuencia de progenitores mieloides comunes (PMC) dentro del compartimento de células progenitoras hematopoyéticas mieloides.
El otro grupo de SMD tenía una mayor frecuencia de progenitores granulocíticos-monocíticos (GMP)dentro del compartimento. En ambos grupos, las poblaciones de células madre mantuvieron la enfermedad durante el tratamiento y se expandieron tras el fracaso de la terapia con HMA, impulsando así la progresión de la enfermedad.
Las expansiones de cada uno de estos tipos de células madre de SMD dependían de la activación de vías de señalización específicas únicas para cada grupo: la vía de supervivencia BCL2 en el grupo CMP y la señalización NF-?B en el grupo GMP.
Como prueba de concepto, los investigadores atacaron farmacológicamente las vías de supervivencia reguladas en modelos preclínicos. El tratamiento de las células del grupo CMP con el inhibidor de BCL2 venetoclax agotó las células madre de SMD in vitro y redujo la carga tumoral en modelos xerográficos derivados de pacientes.
Los investigadores observaron resultados similares al utilizar el inhibidor de NF-?B BMS-345541 en las células del grupo GMP.
A partir de estos resultados, los investigadores evaluaron si los perfiles de las CMH podían predecirlas respuestas al tratamiento en un entorno clínico.
Realizaron un análisis retrospectivo de 21 pacientes de SMD con progresión blástica tras el tratamiento con terapia HMA y venetoclax.
En consonancia con la hipótesis de que la terapia basada en venetoclax se dirige selectivamente alas poblaciones de HSC con el perfi l CMP, los investigadores observaron una disminución significativa de las células madre tras el tratamiento en los pacientes con enfermedad con patrón CMP.
Por el contrario, no hubo cambios significativos en los pacientes con SMD con patrón GMP.
Los pacientes con SMD con patrón CMP tuvieron un tiempo más corto para alcanzar la remisión completa en relación con los que tenían el patrón GMP (1,2 meses frente a 6,5 meses) y una mayor duración de la supervivencia sin recaídas (16,3 meses frente a 5,2 meses).
En conjunto, estos resultados sugieren que los pacientes con SMD con patrón CMP y progresión blástica pueden beneficiarse del tratamiento con el inhibidor de BCL2 altamente selectivo venetoclax.
"Nuestro estudio muestra evidencias tanto preclínicas como clínicas de que los SMD se mantienen gracias a dos perfiles distintos de células madre" subraya la doctora Irene Ganan-Gómez, instructora de Leucemia.
"Esta investigación defiende que el perfil de células madre de los SMD debe ser considerado para determinar los enfoques terapéuticos apropiados dirigidos a estas células, particularmente para la terapia basada en venetoclax".
Advierten de que se necesitan más estudios para establecer si el sistema inmunitario contribuye a la remisión de la enfermedad, y se precisan ensayos prospectivos más amplios para determinar los beneficios selectivos del tratamiento con venetoclax en pacientes con el patrón CMP.
Los investigadores también están probando actualmente la hipótesis de que el tratamiento de otros dos miembros de la familia BCL2 (MCL1 y BCL2A1), ambos efectores de la activación de la vía NFKB, puede superar la progresión de la enfermedad en los SMD con patrón GMP.
"Estos datos tienen el potencial de acelerar el ritmo de los descubrimientos terapéuticos para los SMD, lo que podría beneficiar finalmente a los pacientes con esta enfermedad incurable, señala Colla.
"Se necesitan más estudios, pero estamos entusiasmados por seguir superando los retos asociados al tratamiento de los SMD y la LMA". concluye.
Fuente consultada aquí.