En solo una semana, la paciente pasó de síntomas controlables a fallo multiorgánico, arritmias ventriculares letales y muerte. La autopsia confirmó una infiltración cardíaca masiva por depósitos de amiloide AL.
Una mujer de 71 años con múltiples comorbilidades acudió a urgencias por un cuadro progresivo de disnea y edema en extremidades inferiores.
Los hallazgos iniciales como la elevación marcada del BNP, troponina y dímero D, alertaron sobre una posible afectación cardíaca grave. El electrocardiograma mostraba un patrón sugestivo: bajo voltaje, bloqueo AV de primer grado y ondas Q patológicas en territorio anteroseptal.
La evaluación inicial reveló datos alarmantes: distensión venosa yugular, edemas periféricos y marcadores bioquímicos elevados, incluyendo un BNP de 1714 pg/ml y troponina de 0.21 ng/ml.
El electrocardiograma mostraba un patrón característico con bajo voltaje, bloqueo AV de primer grado y ondas Q patológicas en derivaciones anteroseptales, mientras que el ecocardiograma evidenciaba una hipertrofia ventricular izquierda concéntrica severa (tabique interventricular de 1.5 cm) con patrón restrictivo de llenado diastólico.
Estos hallazgos, junto con la preservación de la fracción de eyección (60-65%), encendieron las primeras alarmas sobre un posible proceso infiltrativo miocárdico.
El estudio se amplió al detectarse hipercalcemia (11 mg/dL) y una paraproteína IgG lambda en la electroforesis de proteínas, con una notable desproporción en las cadenas ligeras (kappa 5.37 mg/dL vs lambda 6535 mg/dL).
La biopsia de médula ósea confirmó la presencia de un mieloma de células plasmáticas con infiltración del 40%, mientras que el estudio esquelético reveló lesiones líticas en huesos largos.
Estos hallazgos hematológicos, en el contexto de la cardiopatía, orientaron hacia una posible amiloidosis AL, aunque en ese momento no se completó la evaluación con técnicas específicas de tinción.
El reingreso una semana después marcó un punto de inflexión en la evolución de la paciente. Presentaba ahora signos de fallo multiorgánico con insuficiencia renal aguda, hepatitis de shock (AST 495 U/L, ALT 494 U/L) y marcada elevación de los biomarcadores cardíacos (BNP 4687 pg/ml, troponina 2.82 ng/ml).
La aparición de taquicardia ventricular polimórfica, con episodios recurrentes a pesar de las medidas de reanimación, reflejaba la gravedad del compromiso miocárdico.
El estudio hemodinámico mostró presiones de llenado severamente elevadas (presión capilar pulmonar enclavada de 40 mmHg) con un índice cardíaco críticamente bajo (1.8 L/min/m2), compatible con shock cardiogénico refractario.
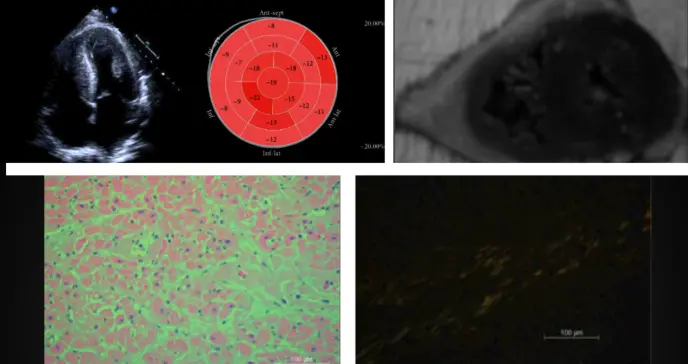
La autopsia proporcionó el diagnóstico definitivo: depósitos de amiloide AL demostrados mediante tinción con rojo Congo en tejido cardíaco y hepático, con la característica birrefringencia verde manzana bajo luz polarizada.
La espectrometría de masas confirmó posteriormente la naturaleza de las proteínas depositadas. Macroscópicamente, se observó cardiomegalia marcada con hipertrofia ventricular izquierda, hallazgos típicos de la afectación cardíaca por amiloidosis.
Según los autores, (Mathews AT,et al.), la amiloidosis cardíaca puede presentarse con diversas manifestaciones cardiovasculares, siendo las más comunes la insuficiencia cardíaca y los trastornos de conducción.
El infiltrado amiloide en el miocardio produce rigidez ventricular que progresa a miocardiopatía restrictiva, caracterizada por disfunción diastólica severa. Los síntomas típicos incluyen disnea de esfuerzo, ortopnea y edema periférico, mientras que las arritmias más frecuentes son la fibrilación auricular (10-20% de casos) y las taquiarritmias ventriculares.
El electrocardiograma en la amiloidosis cardíaca suele mostrar bajo voltaje en derivaciones de extremidades (<5 mm) con pobre progresión de onda R en precordiales. Sin embargo, la ausencia de este patrón no excluye el diagnóstico, ya que solo el 10-20% de pacientes cumplen criterios completos de hipertrofia ventricular izquierda.
La ecocardiografía revela hallazgos característicos como engrosamiento ventricular, disfunción diastólica y el patrón de "cereza en la cima" en el análisis de deformación miocárdica. Este último, con preservación de la deformación apical y afectación de segmentos basales, tiene una sensibilidad del 90-95% para amiloidosis.
La resonancia magnética cardíaca con realce tardío de gadolinio ofrece información pronóstica valiosa, permitiendo clasificar la afectación en patrones subendocárdicos o transmurales, este último asociado con peor pronóstico (5.4 veces mayor mortalidad).
El manejo de la amiloidosis cardíaca requiere un enfoque dual: tratamiento de la enfermedad subyacente (quimioterapia en AL) y manejo de la insuficiencia cardíaca. En casos seleccionados, el trasplante cardíaco o combinado (hígado-corazón en ATTR) puede considerarse, especialmente en pacientes jóvenes sin afectación multiorgánica severa.