La nueva técnica genera fotorreceptores de varilla que se integran en la retina y el cerebro.
Agencia Latina de Noticias de Medicina y Salud Pública
La nueva técnica genera fotorreceptores de varilla que se integran en la retina y el cerebro.
Investigadores financiados por el Instituto Nacional del Ojo (National Eye Institute, NEI) han revertido la ceguera congénita en ratones al cambiar las células de apoyo en la retina llamadas Müller glia en
fotorreceptores de varillas. Los hallazgos avanzan los esfuerzos hacia terapias regenerativas para cegar enfermedades tales como la degeneración macular relacionada con la edad y la retinitis pigmentosa. Un informe de los hallazgos aparece en línea hoy en Nature. NEI es parte de los Institutos Nacionales de Salud.
"Este es el primer informe de los científicos que reprograman la glía de Müller para convertirse en fotorreceptores de barra funcionales en la retina de mamíferos", dijo Thomas N. Greenwell, Ph.D., director del programa NEI para neurociencia de la retina. "Las varillas nos permiten ver con poca luz, pero también pueden ayudar a preservar los fotorreceptores de cono, que son importantes para la visión del color y la agudeza visual alta. Los conos tienden a morir en las enfermedades oculares en etapas posteriores. Si las varillas se pueden regenerar desde el interior del ojo, esta podría ser una estrategia para tratar las enfermedades del ojo que afectan a los fotorreceptores ".
Los fotorreceptores son células sensibles a la luz en la retina en la parte posterior del ojo que señalan al cerebro cuando se activan. En los mamíferos, incluidos los ratones y los humanos, los fotorreceptores no se regeneran por sí solos. Como la mayoría de las neuronas, una vez maduras no se dividen. Los científicos han estudiado durante mucho tiempo el potencial regenerativo de la glía de Müller porque en otras especies, como el pez cebra, se dividen en respuesta a una lesión y pueden convertirse en fotorreceptores y otras neuronas de la retina. El pez cebra puede recuperar la visión después de una lesión retiniana grave. En el laboratorio, sin embargo, los científicos pueden convencer a la glía de Müller de mamíferos para que se comporten más como lo hacen en los peces. Pero requiere herir el tejido.
"Desde un punto de vista práctico, si estás tratando de regenerar la retina para restaurar la visión de una persona, es contraproducente dañarla primero para activar la glía de Müller", dijo Bo Chen, Ph.D., profesor asociado de oftalmología y director. del Programa de Células Madre Oculares en la Escuela de Medicina Icahn en Mount Sinai, Nueva York.
"Queríamos ver si podíamos programar la glía de Müller para convertirnos en fotorreceptores de varillas en un ratón vivo sin tener que dañar su retina", dijo Chen, investigador principal del estudio.
En la primera fase de un proceso de reprogramación en dos etapas, el equipo de Chen estimuló a la glia de Müller en ratones normales para que se dividiera inyectando sus ojos con un gen para activar una proteína llamada beta-catenina. Semanas más tarde, inyectaron en los ojos de los ratones factores que alentaron a las células recién divididas a convertirse en fotorreceptores de varillas.
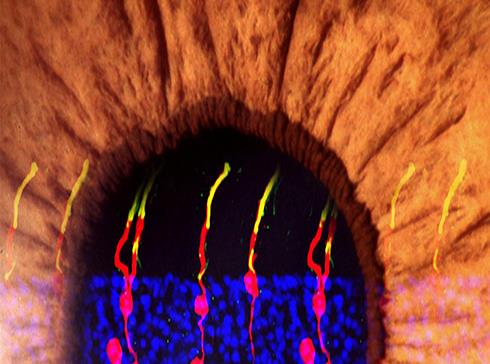
Los investigadores usaron microscopía para rastrear visualmente las células recién formadas. Descubrieron que los fotorreceptores de varillas recién formados no se diferenciaban estructuralmente de los fotorreceptores reales. Además, también se han formado estructuras sinápticas que permiten que las varillas se comuniquen con otros tipos de neuronas dentro de la retina. Para determinar si los fotorreceptores de varillas derivadas de Müller glia eran funcionales, probaron el tratamiento en ratones con ceguera congénita, lo que significaba que nacieron sin fotorreceptores funcionales de varilla.
En los ratones tratados que nacieron ciegos, las varillas derivadas de la glia de Müller se desarrollaron tan eficazmente como en ratones normales. Funcionalmente, confirmaron que las barras recién formadas se comunicaban con otros tipos de neuronas retinianas a través de las sinapsis. Además, las respuestas de luz registradas de las células ganglionares de la retina (neuronas que llevan señales de los fotorreceptores al cerebro) y las mediciones de la actividad cerebral confirmaron que las barras recién formadas se integraban en el circuito de la ruta visual, desde la retina hasta la corteza visual primaria en el cerebro.
El laboratorio de Chen está realizando estudios de comportamiento para determinar si los ratones han recuperado la capacidad de realizar tareas visuales, como una tarea de laberinto de agua. Chen también planea ver si la técnica funciona en tejido de retina humano cultivado.
El estudio fue financiado en parte por NEI otorga R01 EY024986, R01EY021502.